-
Conceptos
-
Elecci�n
del modelo. formulaci�n de la pregunta de investigaci�n
-
Modelos
de endotoxinemia
-
Modelos
de infecci�n bacteriana
-
Modelos
de peritonitis
-
Modelos
que reciben tratamiento
-
Aportaci�n de los modelos precl�nicos al conocimiento de la sepsis humana
-
Conclusi�n
-
Bibliograf�a
Sepsis es la constelaci�n de signos, s�ntomas y cambios
fisiopatol�gicos asociados a una infecci�n. Diferentes est�mulos no
infecciosos (p. ej.: pancreatitis, isquemia-reperfusi�n tras cirug�a
vascular, contusi�n pulmonar, quemaduras masivas, etc.) pueden originar
una respuesta inflamatoria en el hu�sped indistinguible de la originada
por una infecci�n. Esta respuesta inflamatoria se denomina en general
s�ndrome de respuesta inflamatoria sist�mica (SRIS). S�lo cuando el SRIS
se debe espec�ficamente a una infecci�n se denomina sepsis. Sepsis grave
es aquella sepsis que se acompa�a de la disfunci�n de al menos un �rgano.
Las manifestaciones cl�nicas del SRIS que se utilizan
como criterios para su diagn�stico son la taquicardia, la taquipnea o la
necesidad de ventilaci�n mec�nica, la leucocitosis o la leucopenia, y la
fiebre o la hipotermia. Los cambios fisiopatol�gicos asociados al SRIS y a
la sepsis son comunes, y consisten en una respuesta pro-inflamatoria del
hu�sped. En la actualidad, es imposible distinguir cl�nicamente el SRIS y
la sepsis, excepto en los casos en los que existe un foco infeccioso
evidente. La activaci�n por diversos est�mulos (p. ej.: restos de DNA
bacteriano o viral, detritus celulares, endotoxina, componentes de la
pared de bacterias grampositivas, etc.) de una familia de receptores de
membrana denominados Toll-like receptors es el evento molecular com�n al
inicio de la respuesta del hu�sped ante esos insultos causantes del SRIS.
Este reciente descubrimiento ha permitido explicar el hecho de que
diferentes est�mulos conducen a la misma respuesta pro-inflamatoria en el
hu�sped.
La sepsis se asocia, pues, con diferentes cambios en la
funci�n de los �rganos inducidos por un est�mulo infeccioso, en el
contexto de un ambiente pro-inflamatorio. Estos cambios incluyen: (i)
activaci�n de diferentes sistemas de proteasas (coagulaci�n, fibrinolisis,
complemento, elastasa neutr�fila); (ii) hipoperfusi�n tisular; (iii)
vasodilataci�n sist�mica, hipotensi�n sist�mica, vasoconstricci�n pulmonar
y aumento del gasto card�aco; (iv) activaci�n de la glucolisis, lipolisis
y proteolisis; (v) una elevada mortalidad.
A la luz de estos conceptos, un modelo de sepsis
cl�nicamente relevante ha de reproducir una situaci�n pro-inflamatoria en
el animal y alguno de los cambios enunciados previamente tras un est�mulo
infeccioso. Adem�s, remedando la situaci�n cl�nica, debe asociarse a una
mortalidad elevada. La relevancia cl�nica del modelo se basa en que
reproduzca alguno de esos cambios, y en que se acompa�e de una mortalidad
semejante a la sepsis grave humana de forma no aguda (es decir, a lo largo
de los d�as siguientes al est�mulo s�ptico). Ning�n modelo animal reproduce todos los cambios
caracter�sticos de la sepsis humana (Tabla I).
|
Tabla I.
Los modelos animales comparados a la sepsis
humana
|
|
|
|
Caracter�sticas |
Modelos precl�nicos |
Sepsis grave/shock s�ptico en humanos |
|
Edad |
J�venes generalmente |
Adultos o ancianos |
|
Insulto |
Endotoxina o microorganismo definido |
Desconocido o microorganismos m�ltiples |
|
Tratamiento antibi�tico |
Variable |
Siempre |
|
Tiempo del tratamiento |
Antes o poco despu�s del insulto |
Tiempo variable despu�s del insulto |
|
Duraci�n del insulto |
Muy corta (aplicaci�n de LPS en minutos) |
Prolongada (foco s�ptico persistente, episodios de bacteriemia) |
|
Patocronia |
R�pida |
Lenta |
|
Comorbilidad presente |
Casi nunca |
Muy frecuente |
|
Autoanticuerpos |
Desconocido |
Muy frecuente |
|
Uso de ventilaci�n mec�nica |
Variable |
Casi siempre |
|
Limpieza del ambiente |
Deficiente |
Muy limpio |
|
Coprofagia |
Frecuente |
Nunca |
|
Tolerancia a anticoagulantes |
S� |
No |
|
|
Los primates, perros y ratas desarrollan una respuesta
hipodin�mica tras el est�mulo s�ptico. Estas especies son resistentes a la
endotoxina y requieren dosis 10-100 veces superiores a las que inducen una
respuesta en humanos. El conejo es particularmente sensible a la
endotoxina. Los cerdos tambi�n desarrollan una respuesta hipodin�mica. Las
ovejas son m�s sensibles a la endotoxina, y la respuesta pulmonar y
cardiovascular es semejante a la de los humanos.
|
2. Elecci�n
del modelo: formulaci�n de la pregunta de investigaci�n |
El modelo ha de elegirse dependiendo del objetivo que
se pretenda estudiar. Por ejemplo, si se pretende estudiar los mecanismos
de vasodilataci�n ha de usarse un modelo que presente disminuci�n de la
resistencia vascular sist�mica tras el est�mulo. Si se pretende estudiar
la mortalidad, debe ser un modelo cr�nico que presente una mortalidad
significativa durante los d�as siguientes al est�mulo.
La elecci�n del modelo depende de otros factores como
el coste, la familiaridad del personal de investigaci�n con diferentes
especies, la disponibilidad de las instalaciones para estabular animales
grandes, etc. Los animales peque�os (ratas, ratones, conejos) son
apropiados para estudios de mortalidad. La obtenci�n de muestras de sangre
est� limitada por el peque�o volumen sangu�neo de estos animales. Los
animales grandes son m�s apropiados para obtener muestras de sangre m�s
abundantes, y permiten una monitorizaci�n m�s completa (inserci�n de
cat�ter de arteria pulmonar, medici�n de flujos sangu�neos regionales,
etc.). El estudio de la influencia de la dotaci�n gen�tica sobre la
respuesta al insulto es posible en animales peque�os. Por ejemplo, el uso
de la cepa de ratas CH3/HeN, que es una cepa resistente a la endotoxina
(hoy sabemos que debido a una mutaci�n en el Toll-like receptor 4, que
transduce los cambios inducidos por la endotoxina), ha sido de gran
utilidad para estudiar los mecanismos de acci�n de la endotoxina y las
bacterias gramnegativas.
La elecci�n del modelo experimental depende de la
pregunta de investigaci�n planteada. La pregunta plantea la medici�n de un
efecto (variable dependiente) mediante la alteraci�n de otro u otros
factores (variables independientes). La pregunta debe formularse en t�rminos
de una hip�tesis que defina la poblaci�n de estudio, describa
detalladamente las intervenciones, considere la magnitud del efecto
esperado de la intervenci�n, y plantee un curso temporal de los eventos (Fig.1-4):
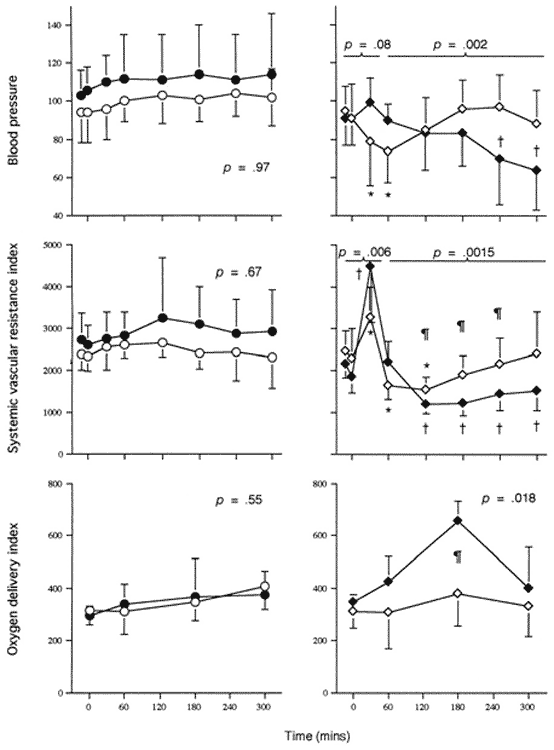
Figura 1. Cambios en diferentes variables hemodin�micas en
ovejas que han recibido en t=0 una dosis i.v. de E. coli en 30 min., y efectos del
tratamiento con L-Arginina. Se observa hipotensi�n transitoria, aumento
marcado seguido de una disminuci�n de la resistencia vascular sist�mica,
sin cambios en el transporte de ox�geno. El tratamiento con L-Arginina se
asocia con una mayor hipotensi�n, con disminuci�n de la resistencia
vascular y con un aumento del transporte de ox�geno (debido a un aumento
del gasto card�aco). Paneles de la izquierda: animales control. Paneles de
la derecha: animales s�pticos. S�mbolos vac�os: no tratados. S�mbolos
llenos: tratados con L-Arginina (Lorente JA, Delgado MA, Tejedor C, Mon E, Herv�s M, Pascual T,
Fern�ndez-Segoviano P, Rieppi G, Soler A, Ayuso D, Esteban A. Modulation
of systemic hemodynamics by exogenous L-arginine in normal and bacteremic
sheep. Crit Care Med 2000; 27: 2474-2479).
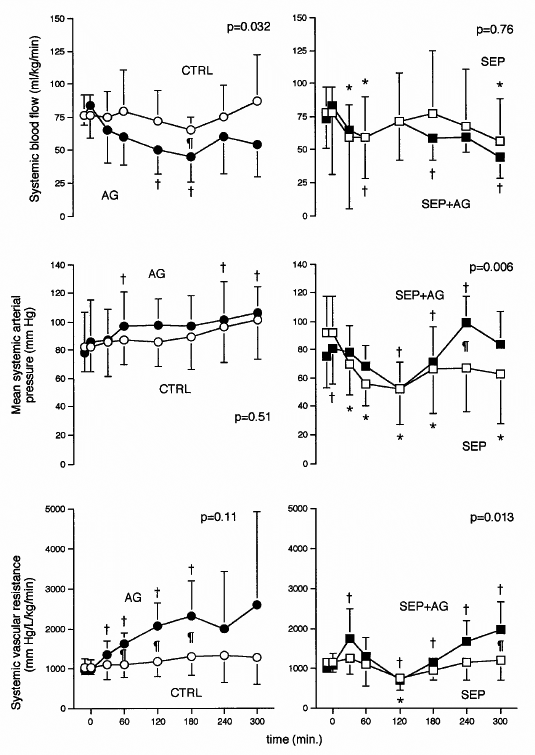
Figura
2.
Cambios en diferentes variables
hemodin�micas en ovejas que han recibido en t=0 una dosis i.v. de E. coli en 30 min.
y tratamiento con aminoguanidina (AG), un inhibidor selectivo de la NO
sintasa inducible. El tratamiento con AG aten�a la hipotensi�n y la
disminuci�n de la resistencia vascular sist�mica asociados a la sepsis.
Paneles de la
izquierda: animales control. Paneles de la derecha: animales s�pticos.
S�mbolos vac�os: no tratados. S�mbolos llenos: tratados con AG
(Lorente JA, Tejedor C, Delgado MA,
Fern�ndez-Segoviano P, Jara N, Tobalina R, Rodr�guez-Corcos A, Moscoso A,
Esteban A. Hemodynamic, biochemical and morphological changes induced by
aminoguanidine un normal an septic sheep.
Intensive Care Med 2000; 26:
1670-1680).
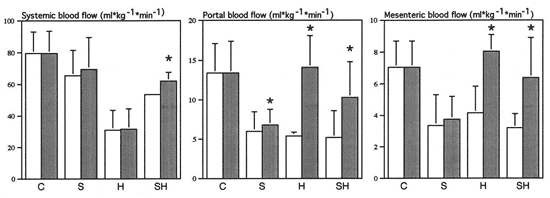
Figura 3. En cerdos s�pticos (E. coli i.v.) la
administraci�n de hemoglobina (Hb) disminuye los flujos regionales por
captaci�n de
NO. El tratamiento con glutation (GSH) aten�a el efecto de la Hb
sobre los flujos regionales, quiz� mediando reacciones de trans-nitrosilaci�n
y aumentando la disponibilidad de NO vasoactivo. C:
control; S:
s�ptico; H:
no s�ptico tratado con Hb; SH:
s�ptico tratado con Hb. Barras vac�as, antes de la administraci�n del GSH.
Barra llenas, despu�s de la administraci�n de GSH. (Tejedor
C, Lorente JA, Delgado MA,
Fernandez-Segoviano P, De Paula M,
Tobalina R, Alonso M, Moscoso A,
Soto F, Blazquez J,
Esteban A. Interaction
between hemoglobin and glutathione in the regulation of blood flow
in normal and septic pigs.
Care Med.
2002; 30: 2493-2500).
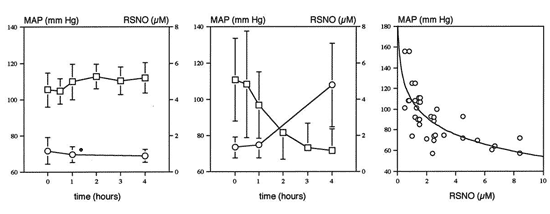
Figura 4. En cerdos s�pticos (E. Coli i.v.) el desarrollo de
hipotensi�n se acompa�a de aumento de la concentraci�n de
nitrosotioles (RSNOs) (compuestos vasoactivos que median la
acci�n del NO) en el suero (Panel central). Los cambios en la presi�n
arterial presentan una correlaci�n con los cambios en la concentraci�n de
RSNOs (Panel derecho). En animales no s�pticos no hay cambios en la
concentraci�n de RSNOs ni en la presi�n arterial media (MAP) (Panel
izquierdo). (Tejedor C,
Lorente JA, Delgado MA,
Fernandez-Segoviano P, De Paula M,
Tobalina R, Alonso M, Moscoso A,
Soto F, Blazquez J, Esteban
A. Interaction between
hemoglobin and glutathione in the regulation of blood flow
in normal and septic pigs.
Care Med.
2002;30:2493-500).
El efecto del tiempo es crucial al considerar la
validez de los diferentes modelos. Se requiere un curso temporal para el
desarrollo de la respuesta del hu�sped al insulto, para que el da�o
secundario al insulto progrese, para que se active la respuesta
inflamatoria, y para que la intervenci�n terap�utica module esos procesos.
2.1. Mecanismos compensadores
La respuesta hemodin�mica caracter�stica de la sepsis
humana es el desarrollo de una circulaci�n hiperdin�mica normo o
hipotensa. Esta respuesta se puede reproducir en ovejas y ratas mediante
ligadura y punci�n del ciego (LPC), mientras que la administraci�n de
bacterias o endotoxina se asocia generalmente con una situaci�n
hipodin�mica. La infusi�n de dosis bajas de endotoxina acompa�ada de
resucitaci�n con fluidos tambi�n produce una respuesta hiperdin�mica [1,
2].
2.2.
Progresi�n de la disfunci�n de los �rganos: efecto del tiempo
La sepsis humana se asocia con disfunci�n secuencial de
�rganos que se presenta a lo largo del tiempo tras el insulto s�ptico.
S�lo los modelos que permiten una monitorizaci�n prolongada a lo largo del
tiempo ofrecen la oportunidad de estudiar la disfunci�n de los �rganos
asociada al insulto s�ptico. Por ejemplo, se puede observar disfunci�n
org�nica en ratas durante las 96 horas tras LPC [3], y cambios en la
permeabilidad capilar pulmonar en ovejas a lo largo de 72 horas tras LPC.
Asimismo, el deterioro de la reactividad vascular y la
disminuci�n y posterior normalizaci�n de la fracci�n de eyecci�n del
ventr�culo izquierdo, cambios caracter�sticos de la sepsis humana y
reproducidos en modelos animales, requieren un tiempo para desarrollarse.
Modelos en los que la mortalidad precoz sea muy elevada
o el tiempo de observaci�n sea reducido no ofrecen la oportunidad para el
desarrollo de disfunci�n de �rganos, y ser�n inadecuados para ciertos
estudios en los que se pretenda estudiar efectos de intervenciones sobre
la aparici�n secuencial de fallo org�nico tras el est�mulo s�ptico.
2.3.
Activaci�n de la respuesta inflamatoria
La respuesta inflamatoria se caracteriza por una
liberaci�n transitoria de TNF- α,
seguida por la liberaci�n de IL-1-β e IL-6. Asimismo, el da�o intestinal
asociado a la sepsis, caracterizado por hipoperfusi�n e hipoxia de la
mucosa intestinal, facilita la translocaci�n de bacterias y toxinas, lo
cual puede amplificar y perpetuar la respuesta inflamatoria durante
per�odos de tiempo prolongados tras el est�mulo s�ptico.
2.4.
Intervenciones terap�uticas
Los modelos de LPC son aptos para la evaluaci�n de
terapias en los cambios fisiopatol�gicos inducidos por la sepsis. Los
modelos agudos de endotoxinemia est�n limitados en general a per�odos
cortos de observaci�n, y permiten evaluar el efecto de intervenciones
terap�uticas sobre cambios precoces tras el est�mulo s�ptico.
El conocimiento en los a�os 50 de que la endotoxina
tiene un papel central en la fisiopatolog�a de la sepsis llev� al
desarrollo de modelos animales en los que se intentaba reproducir algunos
cambios caracter�sticos de la sepsis mediante la administraci�n de
endotoxina. La elevada dosis de endotoxina que se requiere para producir
estos cambios resta relevancia cl�nica a los modelos experimentales. La
administraci�n es en bolos por v�a intravenosa (i.v.) o intraperitoneal (i.p.). Con el objeto de facilitar
que el hu�sped disponga de tiempo suficiente para desarrollar una
respuesta patofisiol�gica al insulto, se puede administrar mediante
infusi�n continua a trav�s de la implantaci�n de una bomba de infusi�n
osm�tica. Este modelo ofrece la ventaja adicional de que se puede estudiar
al animal consciente durante varios d�as.
La respuesta a la endotoxina depende de la especie, y
en algunos aspectos difiere marcadamente de la que caracteriza a la sepsis
humana. En perros, la administraci�n de una dosis letal conduce a
hipotensi�n desde el primer minuto, vasoconstricci�n venosa hep�tica y
disminuci�n del retorno venoso. La presi�n arterial se normaliza durante
la primera hora. Posteriormente, el gasto card�aco y la presi�n arterial
disminuyen y el animal fallece en el contexto de una situaci�n
hipodin�mica [4].
Por el contrario, la administraci�n de endotoxina a
primates subhumanos se asocia con una disminuci�n del gasto card�aco sin
hipotensi�n, y �a diferencia de lo que se observa en pacientes- un aumento
de la diferencia arterio-venosa de ox�geno. La hipotensi�n es un evento
preterminal.
El modelo de endotoxinemia no es propiamente hablando
un modelo de sepsis, pues el est�mulo que conduce a los cambios
fisiopatol�gicos no es infeccioso. La endotoxinemia es, pues, sensu
stricto, un modelo de inflamaci�n sist�mica, m�s que un modelo de sepsis.
Sin embargo, se acepta como modelo para estudiar la fisiopatolog�a de la
sepsis, ya que la endotoxina es una mol�cula central en la fisiopatolog�a
de la sepsis. En el 44% de los enfermos cr�ticos se encuentran niveles
elevados de endotoxina [5], algunos de los cuales presentan infecci�n por
bacterias grampositivas. En estos casos, el origen de la endotoxina
probablemente sea las bacterias gramnegativas de la luz intestinal. Los
niveles de endotoxina se relacionan con el desarrollo de disfunci�n
multiorg�nica y con la mortalidad [6].
3.1.
Modelos de endotoxinemia en roedores
Los modelos de endotoxinemia en roedores presentan
limitaciones adicionales. Las dosis necesarias para producir shock son
10-100 veces superiores a las necesarias en humanos. A diferencia de la hiperglicemia y
el aumento persistente de la gluconeog�nesis encontrada en
humanos, los roedores tratados con endotoxina presentan una hiperglicemia
transitoria que r�pidamente evoluciona hacia una situaci�n de hipoglicemia.
La hipotensi�n inducida por la endotoxina no se debe a vasodilataci�n,
como en humanos, sino que sucede en el contexto de un aumento marcado de
la resistencia sist�mica [7].
Efecto de la dosis
La administraci�n de dosis elevadas de endotoxina a
conejos (5 mg/kg) produce una situaci�n hipodin�mica, mientras que la
administraci�n de dosis menores (1-3 mcg/kg) induce una respuesta
hiperdin�mica semejante a la observada en humanos [8, 9]. En ratas se han
encontrado diferencias semejantes [10, 11].
La mortalidad a las 48 horas puede ser f�cilmente
manipulable mediante la dosis, desde 10% con 5 mg/kg en bolus i.p. hasta 80%
con 20 mg/kg en bolus i.p.
Efecto de la duraci�n de la administraci�n
La administraci�n a ratas de 5 mg/kg en bolus i.p. se
asocia con una mortalidad a las 48 horas del 10%, mientras que la misma dosis
i.p. administrada en 24 horas se asocia con una mortalidad del 0%. La misma
dosis i.v. de 5 mg/kg se asocia con una mortalidad del 0% o del 90%, seg�n
se administre a lo largo de 24 horas o de 4 horas [12, 13].
Tambi�n se ha descrito un modelo de sepsis inducido por
la administraci�n i.v. continua de endotoxina, con el objeto de remedar la
situaci�n cl�nica de endotoxinemia continua. La administraci�n i.v. de
endotoxina a la dosis de 3 mg/d�a produce hipercatabolismo e hipotensi�n,
y es apropiado para el estudio de cambios metab�licos y cardiovasculares
[14].
V�a
de administraci�n
La administraci�n i.v. de endotoxina en ratas produce
una elevaci�n marcada y transitoria de la concentraci�n de endotoxina en
el suero, mientras que la administraci�n por v�a i.p. produce una
elevaci�n m�s progresiva durante las 3 horas siguientes al est�mulo [15].
Modelos de sensibilizaci�n
La sensibilidad a la endotoxina aumenta mediante la
administraci�n previa de ciertos agentes como la D-Galactosamina. Dosis de
100 mcg/kg produce en ratas sensibilizadas una mortalidad semejante
(alrededor del 90% a las 48 horas) que dosis de 15 mg/kg en ratas no
sensibilizadas. Los niveles de TNF a las 2 horas (50 ng/ml) son semejantes en
ratas sensibilizadas y no sensibilizadas, mientras que los niveles de
endotoxina son mil veces inferiores (70 ng/ml versus 70.000 ng/ml)
[16, 17]. Este fen�meno se debe a la sensibilizaci�n de los hepatocitos al
efecto de citoquinas inducidas por la endotoxina, particularmente el TNF- α.
La administraci�n de anticuerpos anti-TNF disminuye la mortalidad de ratas
sensibilizadas que reciben 100 mcg/kg de endotoxina i.p. al 0% [18].
La sensibilizaci�n a los efectos de la endotoxina se
puede conseguir tambi�n mediante la administraci�n previa de plomo,
muramil-dip�ptido o mediante la inducci�n de una infecci�n por bacterias
gramnegativas.
3.2.
Endotoxinemia en ovejas
A diferencia de otras especies (primates, perros,
roedores) la oveja es notablemente sensible a la endotoxina, y presenta
cambios cardiovasculares y pulmonares semejantes a los encontrados
en pacientes con sepsis [19].
El pulm�n de la oveja es, junto con el del caballo, el
m�s semejante anat�micamente al humano. El hecho de que el ganglio
linf�tico mediast�nico caudal recoge, pr�cticamente sin contaminaci�n
sist�mica, s�lo linfa pulmonar permite, mediante la medici�n del flujo
linf�tico, estimar en la ecuaci�n de Starling-Pappenheimer cu�l es el
flujo transvascular de fluido. Por eso, el modelo de f�stula linf�tica
pulmonar cr�nica se ha establecido como el modelo ideal para el estudio
del flujo transvascular pulmonar en condiciones de bacteriemia o
endotoxinemia. Numerosos estudios han demostrado que la administraci�n de
peque�as dosis de endotoxina (1 mcg/kg) o de bacterias produce un aumento
del flujo transvascular pulmonar [20]. Ese modelo ha permitido identificar
dos fases en los cambios circulatorios pulmonares tras la administraci�n
de endotoxina. La fase inicial se caracteriza por hipertensi�n
pulmonar debida a un aumento de la presi�n hidrost�tica capilar y
elevaci�n del tromboxano A2, con formaci�n de edema pobre en prote�nas
[21]. En una segunda fase el edema pulmonar se debe a un aumento de la
permeabilidad y la presi�n en la arteria pulmonar disminuye.
3.3.
Endotoxinemia en humanos
A diferencia de las ratas, los conejos y los humanos
son muy sensibles a peque�as dosis de endotoxina. La administraci�n de 4
ng/kg iv induce un cuadro gripal en 90 min., fiebre y taquicardia, que
alcanzan un m�ximo a las 2-3 horas, y un aumento de la concentraci�n s�rica de ACTH y
adrenalina. Se puede detectar un aumento del TNF desde el minuto
90, que alcanza un m�ximo a las 3 horas, y es indetectable a las 4 horas. Los
niveles de IL-6 e IL-8 alcanzan un pico a las 3 horas post-endotoxina,
mientras que los niveles de IL-1-β e IFN-γ no cambian. La respuesta
hemodin�mica consiste en hipotensi�n, aumento del gasto card�aco y
disminuci�n de la resistencia vascular, cambios que son m�ximos a las 3 horas
post-endotoxina [22-25]. Entre los cambios cardiovasculares que pueden
ser relevantes para la respuesta humana a la sepsis se encuentra una
disminuci�n de la fracci�n de eyecci�n del ventr�culo izquierdo.
La endotoxinemia se asocia con un pico de actividad
t-PA a las 2 horas post-endotoxina, que desaparece hacia la hora 3, seguida de
un aumento de la actividad PAI, que alcanza un m�ximo a las 4-5 horas y
desaparece hacia la hora 24 post-endotoxina. El aumento del PAI coincide
con la aparici�n de signos de activaci�n de la coagulaci�n. El perfil
coagulop�tico consiste, pues, en una activaci�n transitoria de la
fibrinolisis seguida de una fuerte inhibici�n de la fibrinolisis durante
las horas en que la coagulaci�n se encuentra m�ximamente activada. Todos
estos cambios favorecen la formaci�n de dep�sitos de fibrina en la
microcirculaci�n.
Los cambios hemodin�micos y bioqu�micos se normalizan a
las 9 horas tras el est�mulo s�ptico.
4.1.
Infecci�n bacteriana en roedores
La administraci�n de bacterias por diversas v�as en
roedores puede reproducir varios cambios caracter�sticos de la sepsis
humana. Sin embargo, su relevancia cl�nica est� limitada por el hecho de
que estos insultos consisten en la administraci�n de dosis muy elevadas de
bacterias, en modelos en los que el hu�sped es incapaz de localizar la
infecci�n, a diferencia de lo que suele ocurrir en la situaci�n cl�nica.
La administraci�n de E. coli vivos en dosis de 1010 UFC a cobayas
induce una respuesta hipo o hiperdin�mica, seg�n que la administaci�n sea
i.v. o subcut�nea. [26, 27, 28].
La inyecci�n de bacterias vivas por v�a oral o i.p.
induce un estado de sepsis en las ratas. Dependiendo del germen, de la
dosis y de la suspensi�n en la que se vehiculizan los g�rmenes, la
mortalidad puede ser nula [7], o del 100% en 48 horas [29, 30].
4.2.
Modelo de bacteriemia en ovejas y cerdos
Tanto las ovejas como los cerdos se caracterizan por
presentar disfunci�n pulmonar tras la administraci�n i.v. de bacterias.
Este cambio, que no se observa en perros y roedores, se debe probablemente
a la presencia de macr�fagos intravasculares pulmonares [31].
En el modelo porcino no se ha podido inducir una
respuesta hiperdin�mica a pesar de una resucitaci�n con fluidos agresiva
[32]. En ovejas, la infusi�n de P. aeruginosa o endotoxina a lo largo de
30-60 min. se asocia con una respuesta hiperdin�mica tras una corta
respuesta hipodin�mica. La administraci�n de dosis m�s elevadas de
bacterias origina �nicamente una respuesta hipodin�mica.
4.3.
Modelo de bacteriemia en primates
El modelo de sepsis en primates ofrece la ventaja de
que, debido a la proximidad filogen�tica de estas especies con el hombre,
la respuesta cardiovascular y respiratoria es semejante a la presentada
por los humanos. Adem�s, existe reactividad cruzada con numerosas
mol�culas humanas, lo cual facilita la determinaci�n de su concentraci�n.
[33, 34].
La administraci�n intravenosa de E. coli en primates
anestesiados, traqueostomizados y monitorizados hemodin�micamente produce
una bacteriemia que es aclarada de la circulaci�n en 15 minutos tras la
interrupci�n de la infusi�n [35]. Los microorganismos persisten en los
tejidos a las 8 horas de la infusi�n i.v., pero no a las 72 horas post-infusi�n.
La infusi�n i.v. de E. coli en dosis de 2x1010 UFC durante 8 horas en
animales anestesiados y resucitados con Ringer lactato (RL) 5 ml/kg/h. al principio del
experimento, y RL 18-35 ml/kg/hr hacia el final del experimento, se asocia
con una respuesta hiperdin�mica caracterizada por taquicardia, hipotensi�n
y aumento del gasto card�aco. Otros cambios encontrados fueron leucopenia,
trombopenia, acidosis e hipoxemia. Tambi�n se observa liberaci�n de
proteasas (elastasa, catepsina, colagenasa), activaci�n del complejo
terminal del complemento y activaci�n de C3, y signos bioqu�micos de
coagulaci�n intravascular diseminada. El modelo se acompa�a de necrosis
tubular aguda, hepatocitolisis y colestasis. El h�gado, pulm�n, adrenales
e intestino delgado presentan en el examen histol�gico edema, hemorragia y
signos de coagulaci�n intravascular.
Si la dosis administrada de E coli es menor y durante
un per�odo de tiempo de infusi�n m�s corto (5x108 UFC/kg durante 2 horas), se
observa, en comparaci�n con el modelo utilizando una dosis mayor, una
menor hipotensi�n y un menor aumento del gasto card�aco. Los cambios
bioqu�micos y morfol�gicos, y en la funci�n de los �rganos son menos
marcados.
Con el objeto de estudiar el efecto sobre la mortalidad
de intervenciones farmacol�gicas, se ha dise�ado un modelo subcr�nico
consistente en la administraci�n de E coli (2x109 UFC/kg i.v.) durante 2
horas, retornando el animal a su jaula, donde continua intubado,
recibiendo fluidos y soporte ventilatorio si se requiere, durante un
per�odo de observaci�n de 72 horas. La mortalidad de este modelo es elevada,
en torno al 80-90%.
Con el objeto de simular la situaci�n cl�nica en la que
el paciente puede sufrir repetidos episodios de bacteriemia, se ha
dise�ado un modelo subcr�nico en el que el animal recibe 3 dosis de E. coli
(1x108 UFC/kg. el primero, seguido de dos administraciones de 5x107 UFC/kg)
cada 24 horas. Este modelo se asocia con una mortalidad del 50-60%, menor y
m�s tard�a a la asociada a la dosis �nica mayor.
En resumen, el modelo agudo de bacteriemia en
primates es adecuado para el estudio de cambios hemodin�micos asociados al
shock s�ptico. El modelo subcr�nico es pertinente para el estudio de
terapias que tengan un impacto sobre la mortalidad, as� como para el
an�lisis de cambios bioqu�micos y morfol�gicos, que requieren un mayor
per�odo de tiempo para su desarrollo.
5.1.
Peritonitis inducida mediante implantaci�n de bacterias vivas o material
fecal
Otro modelo experimental de sepsis consiste en la
administraci�n i.p. de bacterias vivas o material fecal. La inoculaci�n
fecal de ratas produce una respuesta hipermetab�lica y es letal durante
los siguientes 5 d�as [36]. La administraci�n i.p. de bacterias vivas en
cultivo puro o con un adyuvante produce bacteriemia. Sin embargo, de la
misma forma que la endotoxinemia, en este modelo el hu�sped no tiene
oportunidad de localizar la infecci�n y desarrollar una respuesta completa
compensatoria.
Se puede inducir peritonitis mediante la implantaci�n
de c�psulas de gelatina que contienen sulfato de bario y heces. El sulfato
de bario es un irritante que aumenta la respuesta inducida por las
bacterias. Este modelo se asocia con una elevada mortalidad a las 72 horas
[37].
La peritonitis en perros inducida mediante la
implantaci�n de un co�gulo infectado se realiza mediante la colocaci�n
en el peritoneo de un co�gulo de fibrina que contiene bacterias gramnegativas. El animal puede ser mantenido despierto durante d�as,
sometido a tratamiento antibi�tico y a resucitaci�n con fluidos. La
respuesta cardiovascular consiste en hipotensi�n, disminuci�n del gasto
card�aco y resistencia vascular sist�mica normal, que evoluciona hacia una
situaci�n de aumento del gasto card�aco, normotensi�n y disminuci�n de la
resistencia vascular. La fracci�n de eyecci�n del ventr�culo izquierdo disminuye tras la implantaci�n del co�gulo,
alcanzando un m�nimo al d�a 2-3, para luego nomalizarse hacia el d�a 7.
El modelo permite el estudio de la respuesta de la
funci�n cardiovascular a diferentes dosis del est�mulo s�ptico y a
diferentes intervenciones terap�uticas [38-40].
5.2.
Modelo de ligadura y punci�n del ciego
La ligadura del ciego produce una peritonitis debido a
necrosis del ciego. Sin embargo, estudios posteriores [41, 42] demostraron
que las ratas forman en torno al �rea necr�tica un absceso tabicado que
toleran considerablemente bien, sin mostrar mortalidad en per�odos de
seguimiento de hasta un mes.
La punci�n del ciego antes de retornar el intestino a
la cavidad permite el paso de flora intestinal al peritoneo de una forma
continua, dando lugar a una peritonitis por un mecanismo similar al que
presentan los enfermos con perforaci�n intestinal. El modelo es, pues, de
gran relevancia cl�nica, y presenta una mortalidad f�cil de manipular
variando el tama�o de las perforaciones intestinales.
Estos animales presentan bacteriemia y, debido a la
naturaleza del insulto, tienen tiempo de desarrollar una respuesta. Se
observa una respuesta hiperdin�mica durante las primeras 12 horas tras la LPC,
que evoluciona a un estado hipodin�mico hacia la hora 16-24, presentando
hiperlactatemia, hipoglucemia, y una mortalidad del 95% a las 72 horas.
El modelo es de gran utilidad para estudiar cambios
metab�licos y hemodin�micos de la sepsis, as� como para analizar cambios
en la mortalidad inducidos por diversos tratamientos.
Para optimizar los modelos de sepsis es fundamental
considerar si el animal es tratado de forma similar a un paciente,
incluyendo la reposici�n de volumen, la antibioterapia y el tratamiento
quir�rgico.
La reposici�n de volumen es esencial para mantener la
circulaci�n y el funcionamiento de los �rganos. En los modelos de
endotoxemia, la fluidoterapia modifica la supervivencia y las
caracter�sticas hemodin�micas, y en los modelos con perforaci�n influye de
manera significativa en la respuesta inmunol�gica [43-45]. En la mayor�a
de los estudios de LPC en ratas se administra un bolo �nico o bolos
repetidos de salino fisiol�gico 30-60 ml/kg. por v�a subcut�nea [46-50].
Para remedar de forma m�s precisa la situaci�n cl�nica, en algunos modelos
se administra una infusi�n continua tras el bolo inicial [51-54].
En los animales grandes se puede administrar una dosis
de fluidos fija [55-57] o ajustar la dosis de manera individual [58-61].
La ausencia de fluidoterapia en los modelos de sepsis
causa interacciones serias entre la sepsis y el shock hipovol�mico
subsiguiente. La fisiopatolog�a y la funci�n inmune var�an
significativamente si se administra o no fluidoterapia [62]. A pesar de
ello, algunos autores evitan la administraci�n de fluidos para controlar
mejor las condiciones experimentales, aunque esto ponga en peligro la
validez de los resultados [63].
La administraci�n de antibi�ticos se puede hacer con
dos objetivos: comprobar la eficacia de los mismos en el desarrollo de la
sepsis [64-66] y hacer el modelo m�s cl�nicamente relevante [67-71].
El dise�o experimental en un modelo tratado con fluidos
y antibi�ticos sirve de gu�a para el dise�o de ensayos cl�nicos
posteriores y as� conseguir resultados m�s v�lidos que cuando se emplean
nuevas estrategias en animales no tratados.
La intervenci�n quir�rgica es una parte fundamental del
tratamiento de la sepsis. Por eso, algunos modelos consisten en un
est�mulo s�ptico acompa�ado de un tratamiento quir�rgico, que consiste en
la excisi�n quir�rgica del foco infeccioso y el lavado peritoneal tras LPC
[72-75].
|
7. Aportaci�n
de los modelos precl�nicos de sepsis al conocimiento de la sepsis
humana |
Los modelos pre-cl�nicos de sepsis han contribuido
definitivamente al conocimiento de numerosos aspectos de la sepsis humana.
No se pueden revisar aqu� de forma exhaustiva todos los conocimientos
sobre la sepsis que est�n originados en el estudio de modelos animales,
sino s�lo aquellos que son m�s relevantes, particularmente algunos de los
que han conducido al dise�o de ensayos cl�nicos.
7.1.
Tratamientos anti-inflamatorios
Como es sabido, en casi todos los ensayos cl�nicos
sobre terapias anti-inflamatorias en humanos (inhibidores de la ciclo-oxigenasa,
antagonistas de la IL-1, anticuerpos anti-TNF, antagonistas de la
histamina, etc.) se encuentra en peque�o pero no significativo efecto
beneficioso asociado a la intervenci�n. S�lo analizando todos los estudios
de forma conjunta se encuentra que las diferentes intervenciones
meta-analizadas se asocian con un efecto estad�sticamente significativo
sobre la mortalidad [76-79]. El dise�o de estos ensayos cl�nicos estuvo
basado en estudios pre-cl�nicos en los que se demostraba el papel central
de estas mol�culas en la respuesta del hu�sped a la infecci�n, y en el
hallazgo de que intervenciones que aten�an esta respuesta inflamatoria se
asocian con una mejor supervivencia.
Nosotros hemos revisado todos los estudios realizados
en modelos experimentales de sepsis que analizaron los efectos de terapias
anti-TNF. Este an�lisis ha resultado de gran inter�s, pues permite
identificar en esos estudios pre-cl�nicos �reas de eficacia que fueron
posteriormente encontradas en los ensayos cl�nicos. Tal es el caso de la
mayor eficacia del tratamiento anti-TNF en infecciones bacterianas
gramnegativas en comparaci�n con infecciones grampositivas [80, 81].
Otro hallazgo de inter�s [80] fue que, si bien los
estudios pre-cl�nicos que estudian los efectos de anticuerpos anti-TNF
demuestran eficacia, aquellos en los que se utilizan animales manipulados
gen�ticamente (como animales deficientes en el gen del TNF, deficientes
en el receptor soluble del TNF, o deficientes en el receptor del TNF) no
encontraron efecto protector (la mortalidad en el grupo deficiente no era
inferior a la del grupo normal). Este hallazgo recuerda el resultado de
que en los ensayos cl�nicos en que se utilizaron dosis elevadas de
receptores solubles del TNF la mortalidad empeor� respecto al grupo
control [76].
Asimismo, hemos encontrado que el tratamiento anti-TNF
est� en relaci�n con la mortalidad del grupo control: si la mortalidad es
inferior al 50%, el tratamiento produce da�o; si la mortalidad es superior
al 50%, el tratamiento produce beneficio [80]. Este hallazgo tambi�n ha
sido encontrado en ensayos cl�nicos humanos. Hay por lo menos tres
tratamientos probados en ensayos cl�nicos en humanos cuyo efecto sobre la
mortalidad est� en relaci�n con el efecto del tratamiento: el tratamiento
con el antagonista del receptor de la IL-1, con prote�na C activada y con
anticuerpos monoclonales anti-TNF [81-84].
7.2.
Tratamientos anticoagulantes
Estudios en animales y en humanos demostraron que la
sepsis se acompa�a de un estado sist�mico procoagulante, sentando las
bases para la hip�tesis de que la inhibici�n de la coagulaci�n en la
sepsis humana puede asociarse con una mejor supervivencia [85-91].
El efecto de la terapia anticoagulante en la sepsis
grave ha sido estudiada en ensayos cl�nicos que han investigado el efecto
de la administraci�n de los tres anticoagulantes end�genos fisiol�gicos
(la antitrombina III, la prote�na C activada [PCA] y el inhibidor de la
v�a del factor tisular [TFPI]) [84, 89]. Como es conocido, s�lo el
tratamiento con PCA demostr� eficacia, con un NNT de 16 para salvar una
vida en la poblaci�n de estudio, y un NNT de aproximadamente 6 para salvar
una vida en aquellos pacientes de mayor gravedad de acuerdo con el n�mero
de �rganos en disfunci�n o la puntuaci�n APACHE II (que son aquellos para
los que existe aprobaci�n en Norteam�rica y en Europa).
7.3.
Tratamientos hemodin�micos
El estudio de los mecanismos de hipotensi�n en la
sepsis experimental ha permitido identificar el papel central de la
inducci�n de la �xido n�trico (NO) sintasa inducible (iNOS) en la
hipotensi�n inducida por la endotoxina o por la sepsis. Mientras que el NO
liberado en condiciones fisiol�gicas por la NO sintasa constitutiva (cNOS)
resulta necesario para mantener una homeostasis normal en el hu�sped, el
aumento de la expresi�n de iNOS en la sepsis conduce, entre otros cambios,
a una vasodilataci�n excesiva y a da�o en la funci�n celular mediante la
formaci�n de peroxinitrito, al reaccionar el NO con el radical super�xido
[92-99].
Un ensayo cl�nico en fase II sobre los efectos de la
L-N-monometil-arginina (LNMMA) en pacientes con shock s�ptico demostr� que
esta intervenci�n se asociaba con una mayor proporci�n de enfermos en los
que el shock se resuelve a las 72 horas. En base a estos resultados
esperanzadores, se dise�o un ensayo cl�nico en fase III para analizar los
efectos de esta intervenci�n sobre la mortalidad [100]. Probablemente
debido a cambios en el protocolo, que permit�an aumentar la administraci�n
de LNMMA a dosis mayores y de forma m�s r�pida, se encontr� que el
tratamiento se asociaba de hecho a una mayor mortalidad.
Posteriormente se encontr� en estudios precl�nicos que
la inhibici�n selectiva de la iNOS, respetando la acci�n de la cNOS,
mediante la determinados agentes que presentan una mayor afinidad por la
iNOS que por la cNOS, se asocia a una mejor superviviencia en la sepsis.
Ser�a de gran inter�s probar esta hip�tesis en pacientes con sepsis
[94, 95].
7.4.
Tratamiento ventilatorio
Los modelos de da�o pulmonar agudo han permitido
describir hace a�os el concepto de que el pulm�n sufre un da�o
inflamatorio cuando es sometido a un estr�s c�clico inducido por el uso de
vol�menes corrientes elevados [101, 102]. Estudios posteriores encontraron
que bajo estas condiciones ventilatorias se induce una situaci�n de
inflamaci�n sist�mica. Estos conocimientos pre-clinicos sentaron las
bases para el dise�o de un ensayo cl�nico que comparara el uso de dos
vol�menes corrientes en pacientes con s�ndrome de distr�s respiratorio
agudo o da�o pulmonar agudo. Este estudio encontr� una mayor supervivencia
en los enfermos ventilados con vol�menes corrientes bajos [103].
Interesantemente, ambos grupos no se diferenciaron en el deterioro de la
oxigenaci�n, sino en la duraci�n del fracaso de �rganos no pulmonares y en
la duraci�n del shock.
Estos conocimientos han conducido a la elaboraci�n de
recomendaciones sobre pautas ventilatorias en pacientes con sepsis que
potencialmente minimicen el desarrollo de disfunci�n multiorg�nica y
mejoren la supervivencia.
El avance en el conocimiento de la sepsis y de terapias
eficacias ha sido posible s�lo gracias al desarrollo de modelos pre-cl�nicos
de sepsis [104, 105]. Ning�n modelo reproduce en todos sus aspectos a la
sepsis humana. Sin embargo, cada modelo experimental permite estudiar al
menos los aspectos de la sepsis humana que el animal reproduce.
Aun cuando todo los modelos presentan limitaciones
importantes, es sorprendente la contribuci�n que han hecho al conocimiento
de aspectos fisiopatol�gicos y terap�uticos de la sepsis humana.
Revisiones sistem�ticas de estudios en animales han permitido alcanzar
conclusiones que se asemejan a los resultados de ensayos cl�nicos.
Las recomendaciones para el tratamiento de la sepsis
grave est�n basadas en ensayos cl�nicos que fueron dise�ados en base a un
gran cuerpo de conocimiento procedente de estudios pre-cl�nicos.
El estudio de la sepsis en modelo pre-cl�nicos contin�a
siendo extraordinariamente necesario para avanzar en el conocimiento de la
biolog�a de la sepsis humana y en el dise�o de estrategias terap�uticas
eficaces.
-
Fish RE,
Burns AH, Lang CH, Spitzer JA. Myocardial dysfunction in a nonlethal,
nonshock model of chronic endotoxinemia. Circ Shock 1985; 16: 241-252.
-
Curtis SE,
Cain SM. Regional and systemic oxygen delivery/uptake relations and
lactate flux in hyperdynamic, endotoxin-treated dogs. Am Rev Respir Dis
1992; 145: 348-345
-
Stahl TJ,
Alden PB, Rings WS, Madoff RF, Cerra FB. Sepsis-induced diastolic
dysfunction in chronic canine peritonitis. Am J Physiol
1990; 258: H625-H633.
-
MacLean LD,
Weil MH. Hypotension (shock) in dogs produced by Escherichia coli
endotoxin. Circ Res 1956; 4: 546-556.
-
Danner RL,
Elin RJ, Reilly JM, Hosseini JM, Schlesinger TL, Parrillo JE.
Endotoxemia in human septic shock. Crit Care Med 1988; 16: 317-323.
-
Aasen AO,
Rishovd AL, Stadaas JO. Role of endotoxin and proteases in multiple
organ failure. Progr Clin Biol Res 1989; 308: 305-314.
-
Perkash I,
Satpati P, Agawal KC, Chakravarti RN, Chutani PM. Prolongad peritoneal
lavage and fecal peritonitis. Surgery 1970;68:842-845, Martinez LA,
Quintiliani R, Milton RC. Clinical experience on the detection of
endotoxemia with the limulus test. J Infect Dis 1973; 127: 102-105.
-
Wyler F,
Neutze JM, Rudolph AM. The effects of endotoxin on distribution of
cardiac output in unanesthetized rabbits. Am J Physiol 1970; 219: 246-251.
-
Fink MP,
Morrissey PE, Stein KL, Clement RE, Fiallo V, Gardiner WM. Systemic and
regional hemodynamic effects of cyclo-oxygenase and thromboxane
synthetase inhibition and and hyperdynamic endotoxemic rabbits. Circ
Shock 1988; 26: 41-57.
-
Rackett 1985,
Law WR, Ferguson JL. Naloxone alters organ perfusion during endotoxin
shock in conscious rats. Am J Physiol 1988; 255: H1106-1113.
-
Johnston TD,
Hamptono WH, Fry DE. E. coli endotoxin produces hyperdynamic
hemodynamics in the rat. Circ Shock 1989; 27: 320.
-
Bahrami S,
Schiesser A, Redl H, Schlag G. Comparison of different corticosteroids
in rat endotoxemia. Prog Clin Biol Res 1987; 236: 273-286.
-
McKechnie K,
Furman BL, Parratt JR. Metabolic and cardiovascular effects of endotoxin
infusion in conscious unrestrained rats: effects of methylprednisolone
and BW755C. Circ Shock 1985; 15: 205-215.
-
Fish RE,
Spitzer JA. Continuous infusion of endotoxin from a osmotic pump in the
conscious, unrestrained rat: a unique model of chronic endotoxemia. Circ
Shock 1984; 12: 135-149.
-
Emerson TE,
Fourniel MA, Leach WJ, Edens TB. Protection against disseminated
intravascular coagulation and death by antithrombin III in the
Escherichia coli endotoxemic rat. Circ Shock 1987; 21: 1-14.
-
Freudenberg
MA, Galanos C. Induction of tolerance to lipopolysaccharide (LPS) D-Galactosamine
lethality by pretreatment with LPS is mediated by macrophaes. Infect
Immun 1988; 56: 1352-1357.
-
Freudenberg
MA, Galanos C. Tumor necrosis factor alpha mediates lethal activity of
killed gramnegative and gram positive bacteria in D-galactosamine
treated mice. Infect Immun 1991; 59: 2110-2115.
-
Bahrami S,
Redl H, Buurman WA, Schlag G. Endotoxin shock related disorders
induced by high- versus low-dose lipopolysaccharide (LPS) injection in
rats. Eur Surg Res 1991; 23: S1-60.
-
Traber DL,
Redl H, Schlag G, Herndon DN, Kimura R, Prien T, Traber LD.
Cardiopulmonary responses to continuous administration of endotoxin. Am
J Physiol 1988; 254: H833-H839.
-
Demling RH,
Manohar M, Hill JA. Response of the pulmonary microcirculation to fluid
loading after hemorrhagic shock and resuscitation. Surgery
1980; 87: 552-559.
-
Adams TJ,
Traber DL. The effects of a prostaglandin synthetase inhibitor,
ibuprofen, on the cardiopulmonary response to endotoxin in sheep. Circ
Shock 1982; 9: 481-489.
-
Parker MM,
Shelhamer JH, Bacharach SL, et al. Profound but reversible myocardial
depression in patients with septic shock. Ann Intern Med
1984; 100: 483-490.
-
Parker MM,
Suffrediini AF, Natanson C, Ognibene FP, Shelhamer JH, Parrillo JE.
Responses of left ventricular function in survivors and nonsurvivors of
septic shock. J Crit Care 1989; 4: 19-25.
-
Suffredini
AF, Fromm RE, Parker MM, Brenner M, Kovaks JA, Wesley RA, Parrillo JE.
The cardiovascular response of normal humans to the administration of
endotoxin. N Engl J Med 1989; 321: 280-287.
-
Parker MM,
Shelhamer JH, Natanson C, Alling DW, Parrillo JE. Serial cardiovascular
variables in survivors and nonsurvivors of human septic shock: heart
rate as an early predictor of prognosis. Crit Care Med 1987; 15: 923-929.
-
Durkot MJ,
Wolfe RR. Hyper and hypodynamic models of sepsis in guinea pigs. J Surg
Res 1989; 46: 118-122.
-
Sato T,
Isoyama T, Tanaka J, Jones RT, Cowley RA, Trump BF. The pathophysiology
of septic shock: changes in hemodynamics in rats following live E. coli
injection. An application of the thermodilution method for measurement
of cardiac output. Adv Shcok Res 1982; 7: 25-34.
-
Pass LJ,
Schloerb PR, Pearce FJ, Drucker WR. Cardiopulmonary response of the rat
to gram-negative bacteremia. Am J Physiol 1984; 246: H344-H350.
-
Ahrenholz DH,
Simmons RL. Fibrin and peritonitis I. Beneficial and adverse effects of
fibrin in experimental E. coli peritonitis. Surgery 1980; 88: 41-47.
-
Oderdonk AB,
Weinstein WM, Sullivan NM, Gorbach SL. Experimental intraabdominal
abscesses in rats: quantitative bacteriology of infected animals. Infect
Imunn 1974; 10: 1256-1259.
-
Dehring DJ,
Wismar BL. Intravascular macrophages in pulmonary capillaries of man. Am
Rev Respir Dis 1989; 139: 1027-1029.
-
Mustard RA,
Fisher J, Hayman S, Matlow A, Mullen JBM, Odumeru J, Roomi MW, Scouten
BD, Swanson HT. Cardiopulmonary responses to Pseudomonas septicemia in
swine: an improved model of the adult respiratory distress syndrome. Lab
Anim Sci 1989; 39: 37-43.
-
Hinshaw LB.
Application of animal shock models to the human. Circ Shock
1985; 17: 205-212.
-
Simon GL,
Galfand GA, Connolly RA, O�Donnell TF, Gorbach SL. Experimental
bacteroides fragilis bacteremia in a primate model: evidence that
bacteroides fragilis does not promote the septic shock s�ndrome. J
Trauma 1985; 25: 1156-1162.
-
Schlag G,
Redl H, Hallstr�m S, Radmore K, Davies J. Hyperdynamic sepsis in baboons:
I. Aspects of hemodynamics. Circ Shock 1991; 34: 311-318.
-
Lang CH,
Bagby GJ, Bornside GH, Vial LJ, Spitzer JJ. Sustained hypermetabolic
sepsis in rats: characterization of the model. J Surg Res
1983; 35: 201-210.
-
Weinstein WM,
Onderdonk AB, Barlett JG. Experimental intraabdominal abscesses in rats.
Development of an experimental model. Infec Immun 1974; 10: 1250-1255.
-
Natanson C,
Fink MP, Ballantyne HK, McVittie TJ, Conklin JJ, Parrillo JE. Gram-negative
bacteremia produces both severe systolic and diastolic cardiac
dysfunction that simulates human septic shock. J Clin Invest
1986; 78: 259-70.
-
Fink MP,
MacVittie TJ, Casey LC. Inhibition of prostaglandin synthesis restores
normal hemodynamics in canine hyperdynamic sepsis. Ann Surg
1984; 200: 619-626.
-
Natanson C,
Danner RL, Fink MP, MacVittie TJ, Walker RI, Conklin JJ, Parrillo JE.
Cardiovascular performance with E. Coli challenges in a canine model of
human sepsis. Am J Physiol 1988; 254: H558-H564.
-
Wichterman K,
Baue AE, Chaudry IH. Sepsis and septic shock- a review of laboratory
models and a proposal. J Surg Res 1980; 29: 189-201.
-
Fink MP,
Heard SO. Laboratory models of sepsis and septic shock. J Surg Res
1990; 49: 186-196.
-
Redl H,
Bahrami S, Schlag G, Traber DL. Clinical detection of LPS and animal
models of endotoxemia. Inmunobiol. 1993; 187: 330-345.
-
Fink MP,
Kaups KL, Wang H, Rothschild HR. Maintenance of superior mesenteric
arterial perfusion prevents increased intestinal mucosal permeability in
endotoxic pigs. Surgery 1991; 110: 153-160.
-
Wilson MA,
Chou MC, Spain DA, Downard PJ, Quian Q, Cheadle WG, Garrison RN. Fluid
resuscitation attenuates early citokyne mRNA expression after
peritonitis. J Trauma 1996; 41: 622-627.
-
Wichterman
KA, Baue AE, Chaudry IH. Sepsis and septic shock. A review of laboratory
models and a proposal. J Surg Res 1980; 29: 189-201.
-
Read TE,
Grunfeld C, Kumwenda ZL, Calhoun MC, Kane JP, Feingold KR, Rapp JH.
Triglyceride-rich lipoproteins prevent septic death in rats. J Exp Med
1995; 182: 267-272.
-
Tang C, Liu
MS. Initial externalization followed by internalization of β-adrenegic
receptors in rat heart during sepsis. Am J Physiol 1996; 270: R254-R263.
-
Chen SJ, Wu
CC, Yen MH. Alterations of ex vivo vascular reactivity in
intraperitoneal sepsis. J Cardiovasc Pharmacol 1994; 24: 786-793.
-
Wang P, Ba ZF,
Chaudry IH. Endotelium-dependent relaxation is depressed at the macro
and microcirculatory levels during sepsis. Am J Physiol
1995; 269: R988-R994.
-
Martin CM,
Sibbald WJ, Modulation of hemodynamics and organ blood flow by nitric
oxide synthase inhibition is not altered in normotensive, septic rat. Am
Respir Crit Care Med 1994; 150: 1539-1544.
-
Fox GA,
Paterson NAM, McComark DG. Cyclooxygenase inhibition and vascular
reactivity in a rat model of hyperdinamic sepsis. Am J Physiol
1994; 267: H1377-H1382.
-
Piper RD,
Pitt-Hyde M, Li F, Sibbald WJ, Potter RF. Microcirculatory changes in
rat skeletal muscle in sepsis. Am J Respir Crit Care Med
1996; 154: 931�937.
-
Farquhar I,
Martin CMM, Lam C, Potter R, Ellis CG, Sibbald WJ. Decreased capillary
density in vivo in bowel mucosa of rats with normotensive sepsis. J Surg
Res 1996; 61: 190�196.
-
Goldfarb RD,
Glock D, Kumar A, McCarthy RJ, Mei J, Guynn T, Matushek M, Trenholme G,
Parrillo JE. A porcine model of peritonitis and bacteremia simulates
human septic shock. Shock 1996; 6: 442�451.
-
Arvidsson D,
Almquist P, Haglund U. Effects of Positive end-expiratory pressure on
splanchnic circulation and function in experimental peritonitis. Arch
Surg 1991; 126: 631-636.
-
Fox GA,
Berstein A, LamC, Neal A, Rutledge FS, Inman K, Sibbald WJ. Hematocrit
modifies the circulatory control of systemic and myocardial oxygen
utilization in septic
-
Walker JF,
Cumming AD, Lindsay RM, Solez K, Linton AL. The renal response produced
by nonhypotensive sepsis in a large animal model. Am J Kidney Dis
1986; 8: 88-97.
-
Cumming AD,
Nimmo GR. Hemodynamic, renal and hormonal actions of aprotinin in an
ovine model of septic shock. Crit Care Med 1992; 20: 1134-1139.
-
Hersch M:
Gnidec AA, Bersten AD, Troster M, Rutledge FS, Sibbald WJ. Histologic
and ultrastructural changes in nonpulmonary organs during early
hyperdynamic sepsis. Surgery 1990; 107: 397-410.
-
Fox GA, Lam
CJ, Darragh WB, Neal AM, Inman KJ, Rutledge FS, SibbaldWJ. Circulatory
sequelae of administering CPAP in hyperdynamic sepsis are time dependent.
J Appl Physiol 1996; 81: 976-984.
-
Burchard KW,
Simms HH, Robinson A, DiAmico R, Gann DS. Hypocalcemia during sepsis�Relationship
to resuscitation and hemodynamics. Arch Surg 1992; 127: 265- 272.
-
Barke RA,
Birklid S, Chapin RB, Roy S, Brady PS, Brady LJ. The effect of surgical
treatment following peritoneal sepsis on hepatic gene expression. J Surg
Res 1996; 60: 101-106.
-
Wilkins
TD,Walker CB, Nitzan D, Salyers AA. Experimental infections with
anaerobic bacteria in mice. J Infect Dis 1977; 135: S13-S17.
-
Kresta A,
Shek PN, Odumeru J, Bohnen JMA. Distribution of free and liposome-encapsulated
Cefoxitin in experimental intra-abdominal sepsis in rats. J Pharm
Pharmacol 1993; 45: 779-783.
-
Weinstein WM,
Onderdonk AB, Bartlett JG, Louie TJ, Gorbach SL. Antimicrobial therapy
of experimental intraabdominal sepsis. J Infect Dis 1975; 132: 282-286.
-
DeMarsh PL,
Wells GI, Lewandowski TF, Frey CL, Bhatnagar PK, Ostovic EJR. Treatment
of experimental gram-negative and gram-positive bacterial sepsis with
the hemoregulatory peptide SK&F 107647. J Infect Dis 1996; 173: 203-211.
-
Remick D,
Manohar P, Bolgos G, Rodriguez J, Moldawer L, Wollenberg G. Blockade of
tumor necrosis factor reduces lipopolysaccharide lethality, but not the
lethality of cecal ligation and puncture. Shock 1995; 4: 89- 95.
-
Hotchkiss RS,
Karl IE. Calcium: A regulator of the in�ammatory response in endotoxemia
and sepsis. New Horiz 1996; 4: 58-71.
-
Aranow JS,
Zhuang J, Wang H, Larkin V, Smith M, Fink MP. A selective inhibitor of
inducible nitric oxide synthase prolongs survival in a rat model of
bacterial peritonitis: Comparison with two nonselective strategies.
Shock 1996; 5: 116-121.
-
Cameron EM,
Zhuang J, Nenconi MJ, Phipps R, Fink MP. Dantrolene, an inhibitor of
intracellular calcium release, fails to increase survival in a rat model
of intraabdominal sepsis. Crit Care Med 1996; 24: 1537-1542.
-
Donnenberg
MS: Pathogenic strategies of enteric bacteria. Nature
2000; 406: 768-774.
-
Whang EE,
Dunn JC, Mahanty H, McFadden DW, Zinner MJ, Ashley SW. Endotoxin
inhibitor prevents sepsisinduced alterations in intestinal ion
transport.Am J Surg 1996; 172: 341-344.
-
Refsum SE,
Halliday MI, Campbell G, McCaigue M, Rowlands BJ, Boston VE. Modulation
of TNF� and IL-6 in a peritonitis model using Pentoxifylline. J Ped Surg
1996; 31: 928-930.
-
Wang P, Ba ZF,
Reich SS, Zhou M, Holme KR, Chaudry IH. Effects of nonanticoagulant
heparin on cardiovascular and hepatocellular function after hemorrhagic
shock. Am J Physiol 1996; 270: H1294-H1302.
-
Zeni F,
Freeman B, Natanson C. Anti-inflammatory therapies to treat sepsis and
septic shock: A reassessment. Crit Care Med 1997: 25: 1095-1100.
-
Marshall JC.
Clinical trials of mediator-directed therapy in sepsis: what have we
learned? Intensive Care Med 2000; 26: S75-S83.
-
Marshall JC.
Such stuff as dreams are made of: mediator-directed therapy in sepsis.
Nature Drug Discovery 2003; 2: 391-405.
-
Opal S,
Laterre PF, Abraham E, Francois B, Wittebole X, Lowry S, Dhainaut JF,
Warren B, Dugernier T, Lopez A, Sanchez M, Demeyer I, Jauregui L,
Lorente JA, McGee W, Reinhart K, Kljucar S, Souza S, Pribble J. Trial of
Platelet-Activating Factor Acetylhydrolase in Severe Sepsis
Investigators. Recombinant human platelet-activating factor
acetylhydrolase for treatment of severe sepsis: Results of a phase III,
multicenter, randomized, double-blind, placebo-controlled, clinical
trial. Crit Care Med 2004; 32: 332-341.
-
Lorente JA,
Marshall JC. Can pre-clinical models predict the effects of anti-TNF
therapy in sepsis? (2005, manuscrito en preparaci�n).
-
Panacek EA,
Marshall JC, Albertson TE, Johnson DH, Johnson S, MacArthur FD, Miller
M, et al. Efficacy and safety of the monoclonal anti-tumor necrosis
factor antibody F(ab�)2 fragment afelimomab in patients with severe
sepsis and elevated interleukin-6 levels. Crit Care Med
2004; 32: 2173-2182.
-
Opal SM,
Fisher CJ Jr, Dhainaut JF, Vincent JL, Brase R, Lowry SF, Sadoff JC,
Slotman GJ, et al. Confirmatory interleukin-1 receptor antagonist trial
in severe sepsis. A phase III double-blind, placebo-controlled,
multicenter trial. The I L-1 Receptor Antagonist Study Investigator
Group. Crit Care Med 1997; 25: 115-124.
-
Fisher CJ Jr,
Dhainaut JF, Opal SM, Pribble JP, Balk RA, Slotman GJ, Iberti TJ, et al.
Recombinant human interleukin-1 receptor antagonist in the treatment of
patients with sepsis syndrome. Results from a randomized, double/blind,
placebo/controlled trial. Pahse III rhIL/1ra Sepsis Syndrome Study Group.
JAMA 1994; 271: 1836-1843.
-
Bernard GR,
Vincent JL, Laterre PF et al. Efficacy and safety of recombinant human
Activated Protein C for severe sepsis. N Engl J Med 2001; 344: 699-709.
-
Garcia-Avello
A, Lorente JA, Cesar-Perez J, Garcia-Frade LJ, Alvarado R, Arevalo JM,
Navarro JL, Esteban A. Degree of hypercoagulability and
hyperfibrinolysis is related to organ failure and prognosis after burn
trauma. Thromb Res 1998; 89: 59-64.
-
Lorente JA,
Garcia-Frade LJ, Landin L, de Pablo R, Torrado C, Renes E, Garcia-Avello
A. Time course of hemostatic abnormalities in sepsis and its relation to
outcome. Chest 1993; 103: 1536-1542.
-
Levi M.
Sepsis and the coagulation system. Advances in Sepsis 2000; 1: 16-22.
-
Garcia-Frade
LJ, Lorente JA, Garcia-Avello A, de Pablo R, Landin L. Plasminogen
activator inhibitor-1 levels determine the profibrinolytic response in
disseminated intravascular coagulation. Am J Hematol 1992; 41: 303-304.
-
Warren BL,
Eid A, Singer P et al. Caring for the critically ill patient. High-dose
antithrombin III in severe sepsis: A randomized controlled trial. JAMA
2001; 286: 1869-1879.
-
Dhainaut JF,
Yan SB, Margolis BD, Lorente JA, Russell JA, Freebairn RC, Spapen HD,
Riess H, Basson B, Johnson G 3rd, Kinasewitz GT; PROWESS Sepsis Study
Group. Drotrecogin alfa (activated) (recombinant human activated protein
C) reduces host coagulopathy response in patients with severe sepsis.
Thromb Haemost. 2003; 90: 642-53.
-
Taylor FB Jr,
Chang A, Esmon CT et al. Protein C prevents the coagulopathic and lethal
effects of Escherichia coli infusion in the baboon. J Clin Invest
1987; 79: 918-925.
-
Landin L,
Lorente JA, Renes E, Canas P, Jorge P, Liste D. Inhibition of nitric
oxide synthesis improves the vasoconstrictive effect of noradrenaline in
sepsis. Chest. 1994; 106: 250-256.
-
Lorente JA,
Landin L, De Pablo R, Renes E, Liste D. L-arginine pathway in the sepsis
sy ndrome. Crit Care Med. 1993; 21: 1287-1295.
-
Liaudet L,
Soriano FG, Szabo C. Biology of nitric oxide signaling. Crit Care Med
2000; 28: 37-52.
-
Lorente JA,
Tejedor C, Delgado MA, Fernandez-Segoviano P, Jara N, Tobalina R,
Rodriguez-Corcos A, Moscoso A, Esteban A. Hemodynamic, biochemical and
morphological changes induced by aminoguanidine in normal and septic
sheep. Intensive Care Med 2000; 26: 1670-1680.
-
Lorente JA,
Delgado MA, Tejedor C, Mon E, Herv�s M, Pascual T, Fern�ndez-Segoviano
P, Rieppi G, Soler A, Ayuso D, Esteban A. Modulation of systemic
hemodynamics by exogenous L-arginine in normal and bacteremic sheep.
Crit Care Med 2000; 27: 2474-2479.
-
Lorente JA,
Tejedor C, Fern�ndez-Segoviano P, Delgado MA, Tobalina R, Mon E, et al.
Interaction between exogenous purified hemoglobin and the low molecular
weigth glutathion in the regulation of vascular tone in normal and
septic pigs. Crit Care Med 2002; 30: 2493-2495.
-
Lorente JA,
Landin L, Renes E, De Pablo R, Jorge P, Rodena E, Liste D. Role of
nitric oxide in the hemodynamic changes of sepsis. Crit Care Med
1993; 21: 759-767.
-
Lorente JA,
Landin L, Canas P, Delgado MA, Albaya A, Renes E, Jorge P, Liste D.
Effects of nitric oxide synthase inhibition on the cardiovascular
response to low output shock. Crit Care Med 1996; 24: 482-487.
-
Lopez A,
Lorente JA, Steingrub J, Bakker J, McLuckie A, Willatts S, Brockway M,
Anzueto A, Holzapfel L, Breen D, Silverman MS, Takala J, Donaldson J,
Arneson C, Grove G, Grossman S, Grover R. Multiple-center,
randomized, placebo-controlled, double-blind study of the nitric oxide
synthase inhibitor 546C88: effect on survival in patients with septic
shock. Crit Care Med 2004; 32: 21-30.
-
Dreyfuss D,
Basset G, Soler P et al. Intermittent positive-pressure hyperventilation
with high inflation pressures produces pulmonary microvascular injury in
rats. Am Rev Respir Dis 1985; 132: 880-884.
-
Dreyfuss D,
Saumon G. Ventilator-induced lung injury: lessons from experimental
studies. Am J Respir Crit Care Med 1998; 157: 294-323.
-
The acute
respiratory distress syndrome network. Ventilation with lower tidal
volumes as compared with traditional tidal volumes for acute lung injury
and the acute respiratory distress syndrome. N Engl J Med. 2000;
342: 1301-1308.
-
Freise H,
Br�ckner UB, Spiegel HU. Animal models of sepsis. J Invest Surg
2001; 14: 195-212.
-
Esmon CT. Why do animal models of sepsis
(sometimes) fail to mimic human sepsis. Crit Care Med 2004; 32: S219-S222.
Natalia Ramos, Fundaci�n de Investigaci�n Biom�dica
Jos� A. Lorente Balanza, Servicio de Medicina
Intensiva
Hospital
Universitario de Getafe, Madrid
�REMI,
http://remi.uninet.edu. Mayo 2005.
Palabras clave:
Sepsis, Shock s�ptico, Modelos experimentales.
Busque en REMI con Google:
Env�a tu comentario para su
publicaci�n |